
por Helio Magarinos Torres Filho, diretor médico
Desde o início da pandemia Covid-19, os testes laboratoriais têm sido de fundamental importância, tanto para o diagnóstico, como para o acompanhamento e prognóstico de pacientes afetados. Muitas tecnologias novas foram desenvolvidas em tempo recorde e, atualmente, já são tantas que resolvemos fazer um resumo abaixo com a finalidade de melhor orientar sobre indicação dos testes disponíveis.
Diagnóstico
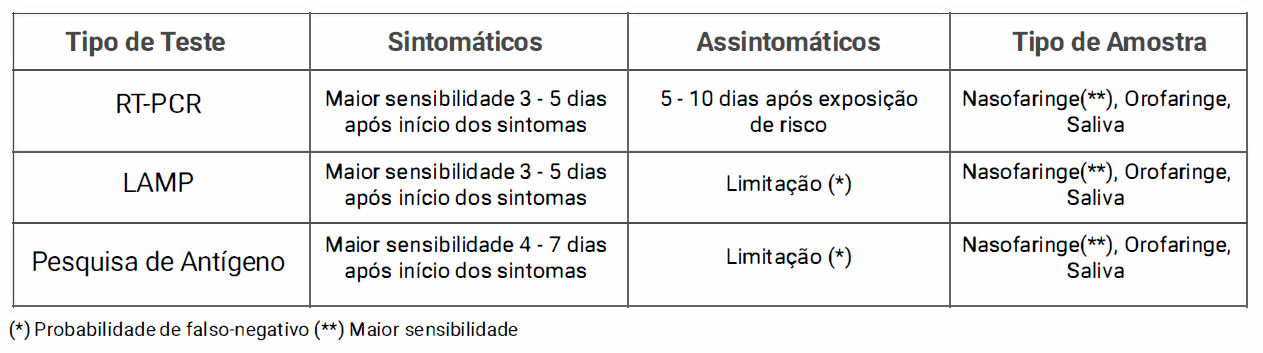
Para a confirmação diagnóstica, assim como o rastreio em assintomáticos o teste considerado como padrão, por ser o mais sensível e específico, ainda é o RT-PCR (Reverse Transcription Polymerase Chain Reaction), que é o teste que utiliza a amplificação do material genético alvo que possa estar contido na amostra, como método de detecção. Outros tipos de testes moleculares também foram introduzidos, sendo o mais utilizado LAMP (Loop-Mediated /sothermal Amplification), que, em resumo, consiste em um teste também de amplificação do material genético, mas utilizando reação isotérmica, o que o difere do RT-PCR em que ocorre a variação de temperatura a cada ciclo. A diferença básica entre os dois testes está em um grau de sensibilidade um pouco melhor para o RT-PCR, observado principalmente em pacientes assintomáticos, nos quais os ciclos de amplificação (CT, Cyc/e Tresho/d) se encontram maiores, o que se traduz em uma menor quantidade de material genético virai na amostra. A quantidade de CTs necessários para a detecção é inversamente proporcional à quantidade de vírus. Quanto menor o CT, maior a quantidade. O LAMP - PCR portanto, tem grau de sensibilidade suficiente para a detecção na maioria dos casos, com exceção daqueles em que o CT se apresenta elevado, mais comum em pacientes assintomáticos. Dentre ambos os tipos de testes moleculares, temos os testes de resultados mais rápidos e os principais exemplos são Xpress, GeneXpert (Cepheid, EUA) - RT-PCR e o ID-Now (Abbott, EUA) - LAMP. Em modo geral, os testes de diagnóstico molecular rápido têm grau de sensibilidade semelhante ou até superior aos testes moleculares tradicionais, como é o caso do GeneXpert.
Outro tipo de teste que passou a ser utilizado é a pesquisa de antígeno, que consiste basicamente na pesquisa de proteínas virais, sem haver amplificação e, portanto, com menor grau de sensibilidade. Estudos mais recentes mostram que a nova geração deste tipo de teste tem boa performance, próxima à dos testes por biologia molecular, quando realizados em pacientes sintomáticos. Para casos de pacientes assintomáticos, com CT elevado, os resultados negativos devem ser vistos com ressalvas, devido à possibilidade de resultados falso-negativos.
O tipo de amostra utilizado também sofreu avanços. A amostra padrão que ainda apresenta maior grau de sensibilidade é o raspado de Nasofaringe; entretanto, outros tipos como raspado de orofaringe e saliva também podem já ser utilizados. Assim como acontece com os testes, as amostras de saliva podem ter grau de sensibilidade ligeiramente inferior ao do raspado de nasofaringe; o que também vai estar relacionado à quantidade de conteúdo virai da amostra (CT) e, portanto, ao estágio clínico da doença, sendo mais recomendado a utilização em pacientes sintomáticos, ou seja, resultados negativos em pacientes assintomáticos devem ser vistos com cautela e requer uma boa correlação clínico-laboratorial. Na nossa opinião, os testes em saliva devem ser reservados para casos especiais nos quais existem maiores dificuldade para a coleta em nasofaringe, como crianças e pessoas que suportam mal o desconforto da coleta em nasofaringe.
Testes sorológicos para diagnóstico: Apesar da evolução dos testes para a pesquisa de anticorpos, principalmente em relação à especificidade, ainda existe a limitação do período para a realização do teste. A maioria dos estudos mostram que, apesar de poder haver a detecção de anticorpos já a partir do 7° dia após o início dos sintomas, o maior grau de sensibilidade só será atingido após o 14° ou até mesmo 21 ° dia. Este tipo de teste continua com a indicação para ser realizado naqueles casos em que não foi possível a realização do teste diagnóstico direto, ou quando, apesar da permanência da suspeita clínica, o teste direto foi negativo. Ainda permanece, entretanto, a superioridade dos testes realizados em plataformas automatizadas, frente aos testes imunocromatográficos, respectivamente conhecidos como sorologia e teste rápido.
Acompanhamento e prognóstico da doença
A covid-19 é uma condição clínica em que teremos muitos biomarcadores alterados, principalmente por se tratar de um estado inflamatório, por vezes generalizado. De cerca de 25 marcadores biológicos utilizados, alguns, segundo estudos de metanálise, estão melhor correlacionados com agravamento do estado clínico e morte do que outros. As dosagens de lnterleucina 6, Proteína e-Reativa, Leucometria e Linfocitometria, se correlacionam melhor com o grau de inflamação, enquanto D-dímeros e Fibrinogênio, são melhores marcadores de estados pró trombóticos. O TAP e PTT não têm grande utilidade nestes casos. Já para a avaliação cardíaca, deve ser utilizada a Troponina de Alta Sensibilidade (Tn-AS), LDH, BNP/NT-Pro-BNP e CK, sendo a Tn-AS o melhor marcador. Devemos ainda lembrar que a elevação da Tn-AS pode ser derivada de Isquemia (1AM), hipóxia severa, sepse, inflamação sistêmica, tromboembolismo pulmonar ou Cardiomiopatia/Miocardite de Estresse. Existe evidência de que aumentos consideráveis nos níveis de Tn-AS possam estar associados a elevação de evidência de que aumentos consideráveis nos níveis de Tn-AS possam estar associados a elevação de até 8 vezes do risco para morte. E também que as elevações de Tn-AS ao longo do tempo, sem os sinais típicos na Ecocardiografia e ECG, estão relacionadas à inflamação sistêmica. Além disso, vale a pena lembrar que valores de Tn-AS detectáveis, mesmo estando abaixo do ponto de corte, também podem ter valor prognóstico e merecem acompanhamento.
Exames pós-vacina
Não existe indicação formal para a realização da pesquisa de anticorpos contra SARS-CoV-2 pós-vacinai para todos que tomarem vacina; entretanto, em alguns casos especiais, a pesquisa dos anticorpos pode ser de utilidade clínica, principalmente em grupos mais vulneráveis que possam vir a ter novos contatos de risco.
Assim, como existem vacinas com diferentes princípios ativos, também temos testes para a pesquisa de anticorpos que utilizam princípio antigênicos diferentes. Vacinas como a Coronavac e a Covaxin, por exemplo, utilizam vírus inativado como princípio ativo, enquanto outras como a Astra-Zeneca Oxford e a Sputilnik V, utilizam a proteína S (spike) com vetor virai, e também Pfizer e Moderna, que utilizam RNAm sintético. Em resumo, os testes para a pesquisa de anticorpos que utilizam a proteína S RBD como antígeno funcionam para todas as vacinas até então disponíveis; já os testes que utilizam a proteína N como antígeno só irão funcionar para as vacinas que utilizam o vírus inativado. O motivo é que tanto as vacinas que usam vetor virai, como as que usam RNAm sintético, utilizam a proteína S como princípio ativo e, consequentemente, os testes que usam proteína N como antígeno não serão capazes de detectar os anticorpos contra a proteína S, que serão formados por estas vacinas. Já as vacinas que usam vírus inativado, terão seus anticorpos detectados por qualquer tipo de teste, já que os indivíduos que as recebem, desenvolverão anticorpos contra o vírus como um todo e não apenas para uma região específica. O teste indicado para a verificação da produção de anticorpos pós-vacina seria a Pesquisa de lgG para proteína S do SARS-CoV-2, pois este vai funcionar com todas as vacinas. No Richet, todos os testes utilizam a proteína S como antígeno.
Outro tipo de teste que também pode ser de utilidade pós-vacina é a Pesquisa de Anticorpos Neutralizantes para SARS-CoV-2, através de uma metodologia conhecida como sVNT (surrogate virai neutralizing test). O teste, conhecido como cPass (GeneScript) é capaz de medir a presença de anticorpos neutralizantes na amostra, a partir da inibição da ligação entre a região S1 RBD do SARS-CoV-1 com o receptor ACE2 celular. Estudos indicam que o teste apresenta grau de sensibilidade e especificidade superiores aos testes de pesquisa de anticorpos lgG contra SARS-CoV-2 e com acurácia superior a 85%, quando comparado com os testes tradicionais de neutralização virai. Recentemente, outro teste do tipo sVNT foi disponibilizado, Eco F ncovid Ab (Eco Diagnóstica, Brasil), com o mesmo princípio, que apresenta maior facilidade de execução e resultados mais rápidos. A limitação em relação aos testes sVNT é que um resultado negativo não necessariamente pode significar ausência de neutralização virai, já que existem outros mecanismos de neutralização que não são detectados por este tipo de teste.
Acreditamos que a melhor indicação para a pesquisa de anticorpos pós-vacina covid-19 seja a Pesquisa de Anticorpos lgG para proteína S do SARS-CoV-2 e a Pesquisa de Anticorpos Neutralizantes para SARS-CoV-2, pois obteremos o maior grau de sensibilidade e de especificidade.
Quando realizar a pesquisa de anticorpos pós-vacina?
O período recomendado para a realização da pesquisa de anticorpos pós-vacina é após a 3ª ou 4ª semana da tomada da segunda dose da vacina.
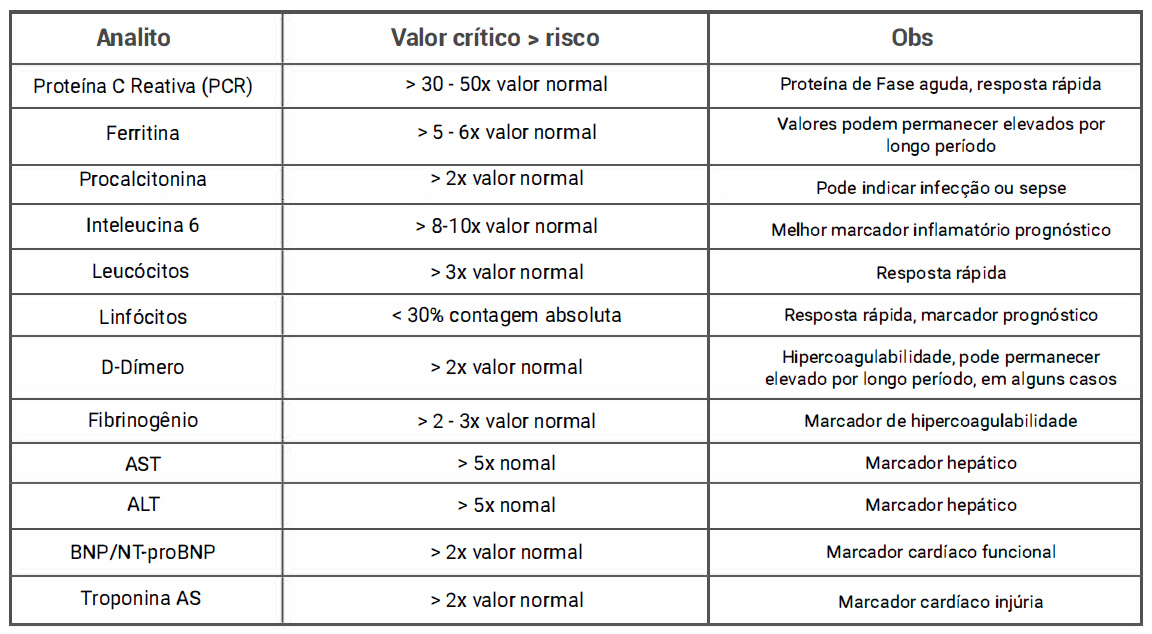
Tabela listando os tipos de vacinas disponíveis com os tipos de testes de anticorpos para Covid-19:

Tabela listando os tipos de vacinas disponíveis com os tipos de testes de anticorpos para Covid-19:

Tabela de testes comercialmente disponíveis e aplicação com as vacinas:

Tabela de testes comercialmente disponíveis e aplicação com as vacinas:

Interferência das novas variantes de SARS-CoV-2 nos testes diagnósticos
Até o momento não existe evidência de que as novas variantes possam interferir nos testes diagnósticos para covid-19 utilizados no Brasil.
Referências:
1. Meyer B et ai, Validation and clinicai evaluation of a SARSCoV-2 surrogate virus neutralisation test (sVNT), Emerging Microbes & lnfections 2020, VOL. 9 https://doi.org/10.1080/22221751.2020.1835448
2. Taylor C S et ai, A New SARS CoV-2 Dual Purpose Serology Test: Highly Accurate lnfection Tracing and Neutralizing Antibody Response Detection, J Clin Microbial doi:10.1128/JCM.02438-20 jan 2021
3. Rhein C V et ai, Comparison of potency assays to assess SARS-CoV-2 neutralizing antibody capacity in COVID-19 convalescent plasma, Journal of Virological Methods 288 (2021) 114031
4. Patel U E et ai, Comparative Performance of Five Commercially Available Serologic Assays To Detect Antibodies to SARS-CoV-2 and ldentify Individuais with High Neutralizing Titers, February 2021 Volume 59 lssue 2 e02257-20 Journal of Clinicai Microbiology
5. Martins-Filho, P R et ai, Biomarcadores de Lesão Miocárdica e Complicações Cardíacas Associadas à Mortalidade em Pacientes com COVID-19, Sociedade Brasileira de Cardiologia, Comunicação Breve, jun 2020, 001: https://doi.org/10.36660/abc.20200372
6. Chaudhary R et ai, Thrombo-inflammatory Biomarkers in COVID-19: Systematic Review and Metaanalysis of 17,052 patients, Mayo Clinic Proceedings, jan 2021, https://doi.org/10.1016/j.mayocpiqo.2021.01 .009
7. Marca A L et ai, Testing for SARS-CoV-2 (COVID-19): a systematic review and clinicai guide to molecular and serological in-vitro diagnostic assays, RBMO VOLUME 41 ISSUE 3 2020, https://doi/
8. Procop G W et ai, A Comparison of Five SARS-CoV-2 Molecular Assays With Clinicai Correlations, Am J Clin Pathol 2021 ;155:69-78 001: 10.1093/ajcp/aqaa181
