
As infecções do trato respiratório inferior constituem uma das maiores causas de internação hospitalar, com elevado índice de morbidade e de mortalidade, principalmente em populações mais suscetíveis, como idosos, crianças < 5 anos de idade, portadores de doenças crônicas e pacientes sob uso de ventilação mecânica. A OMS estima que as Pneumonias Adquiridas na Comunidade (PAC) tenham sido a causa de cerca de 3 milhões de mortes, em todo o mundo, no ano de 2016. O isolamento do agente etiológico é de fundamental importância para a administração do antimicrobiano alvo e estudos indicam que a entrada com antibióticos em até 4 horas após a abertura do quadro clínico, pode reduzir consideravelmente o grau de mortalidade, daí a necessidade de antibioticoterapia de largo espectro empírica, até que se tenha os resultados microbiológicos definitivos. Em se tratando de pacientes hospitalizados com suspeita de Pneumonia Adquirida no Hospital (PAH) ou Pneumonia Adquirida por Ventilação Mecânica (PAV), o quadro torna-se ainda mais premente, pois existe grande possibilidade do envolvimento de germes portadores de multirresistência, cujos graus de mortalidade são consideravelmente elevados.
Historicamente, os testes utilizados para o diagnóstico etiológico são as culturas para aeróbios, anaeróbios, fungos e, se indicado, também micobactérias, além das pesquisas diretas pelas colorações de Gram, Giemsa e Zihel-Nielsen (BAAR). Adicionalmente, pode-se acrescentar testes moleculares para a pesquisa de vírus, mas estes não fazem parte das rotinas e têm de ser solicitados separadamente. A introdução de testes mais rápidos como o GeneXpert (Cepheid, EUA) para M. tuberculosis e Vírus Influenza, como também o painel de Vírus Respiratórios (Filmarray Biofire, BioMérieux, EUA), que detecta a presença de material genético dos 17 vírus respiratórios mais comuns e 4 bactérias (B. pertussise B. parpertussis, M. pneumoniaee C. pneumoniae), vêm modicando consideravelmente o diagnóstico das infecções virais respiratórias. Mais recentemente, com o advento da pandemia por Covid-19, também tivemos a introdução do GeneXpert para SARS-CoV-2 que tem trazido grande agilidade ao diagnóstico em casos especiais. Outros testes também utilizados incluem as pesquisas de antígenos urinários para S. pneumoniae e L. pneumophila, de boa sensibilidade, mas especificidade variável conforme a fase da doença. Entretanto, nos casos de pneumonias bacterianas, que são as mais frequentes em pacientes hospitalizados, ainda não tínhamos testes moleculares rápidos, não pelo menos na forma de painéis. Por outro lado, a sensibilidade dos testes tradicionais, mesmo utilizando as melhores técnicas disponíveis, podem deixar de detectar os agentes etiológicos em cerca de 30% ou mais dos casos, o que corrobora a utilização de antibioticoterapia empírica. A baixa sensibilidade das culturas pode ser explicada pela utilização prévia de antimicrobianos e também pela contaminação com a flora bacteriana local.
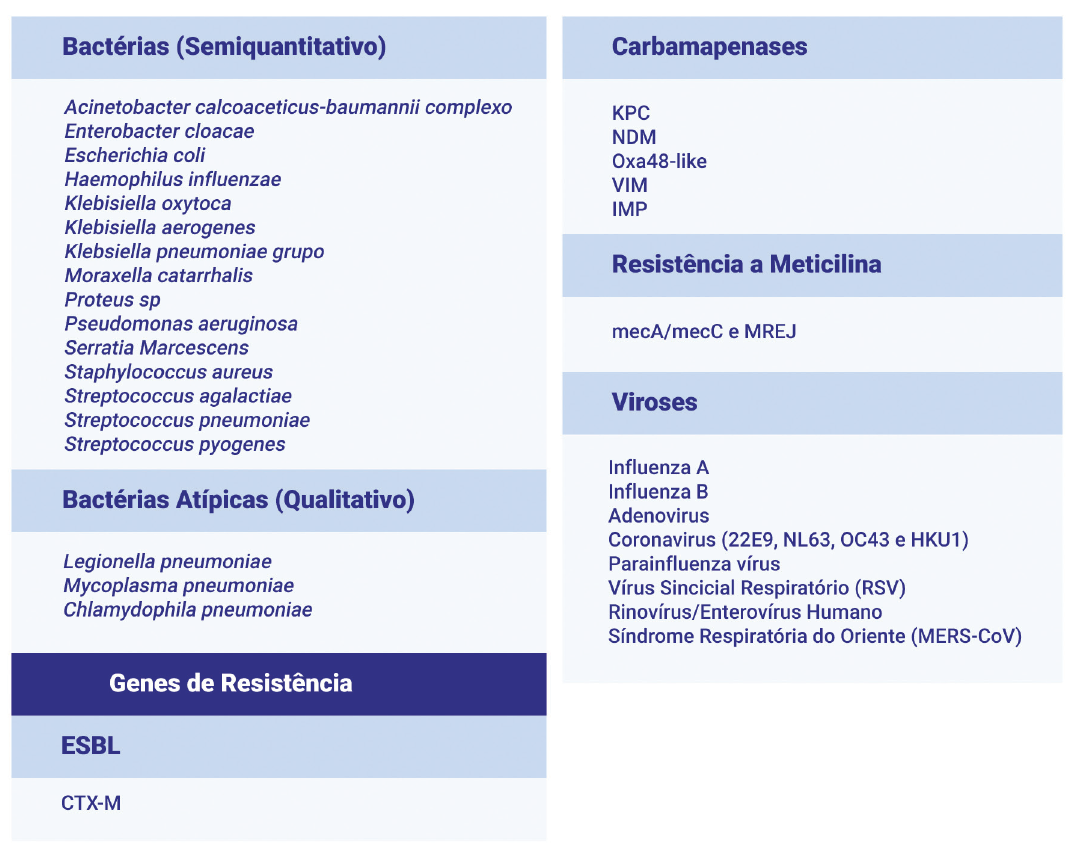
O novo Painel Molecular Pneumonia (Biofire Filmarray, BioMérieux, EUA) é capaz detectar 34 alvos, incluindo o material genético tanto das principais viroses respiratórias, como também das principais bactérias envolvidas em pneumonias, além também das principais mutações que conferem multirresistência. O teste também fornece um resultado semiquantitativo, o permite distinguir o achado de germes ocasionais dos causadores de infecção (só será reportado se houver quantidade superior a 10³ CFU/mL). A detecção de sites de multirresistência, apesar de ser independente da detecção de bactérias, só é reportada se houver o germe correspondente (ex: mecA/mecC e MERJ só reportado se houver presença de S. aureus, assim como ESBL e carbamepenases só são reportados na presença de germes produtores, como Enterobacter, Klebsiella, Pseudomonas, etc.).
O teste pode ser realizado em amostras diretas de escarro, aspirados brônquicos e lavado broncoalveolar (LBA).
A performance clínica do teste, que já vem sendo utilizado na rotina microbiológica em outras localidades como EUA e Europa, tem sido comprovada através de diversos estudos publicados. Desses, podemos citar o estudo feito em Taiwan (Lee S H et al, J Microbiol Immuno Infect, 2019), com 59 amostras de aspirado brônquico e lavado broncoalveolar, no qual, quando comparado com métodos tradicionais como cultura e testes moleculares, obtiveram índice de concordância em resultados positivos (PPA) e de concordância com resultados negativos (NPV) de 90% e de 97,4%, respectivamente. Além disso, o estudo demonstrou codetecção (mais de 1 patógeno incluindo bactérias e vírus) em 42,3% das amostras. E, como conclusão, a utilização do Painel Filmarray Pneumonia permitiu a mudança da prescrição de antibióticos em 43,7% dos casos. Outros estudos, como o Murphy C N et al, J Clin Microbiol, 2020, no qual foi avaliada a performance do teste em comparação com os métodos tradicionais, analisando 846 amostras de LBA e 836 de escarro, coletadas em 8 centros dos EUA, mostrou sensibilidade e especificidade > 95% e 90%, respectivamente, para a maioria dos germes detectados pelo painel. Outro estudo (Buchan B W et al, J Clin Microbiol, 2020), utilizando 1600 amostras de LBA e escarro, coletadas de 8 centros dos EUA, mostrou PPA e NPA de 96,2% e 98,7%, respectivamente, além da codetecção de vírus e bactérias em 39% das amostras. A revisão dos prontuários médicos apontou um potencial de ajustes na antibioticoterapia em 70% dos casos, incluindo a suspenção ou descalonamento em 48% dos casos. Em todos os estudos, houve discrepância na quantificação do teste molecular coma das culturas, atribuído a uma maior sensibilidade dos testes moleculares, incluindo a possibilidade da detecção de germes inviáveis, com material genético remanescente. Entretanto, nas amostras que mostravam maior quantidade de germes (> 10? CFU/mL), houve muito boa correlação.
Como conclusão, o novo Painel Molecular Pneumonia demonstra um grande potencial de auxílio no combate às pneumonias, desde que seja utilizado nos casos em que haja indicação clínica precisa e sempre se fazendo boa utilização da correlação clínica-laboratório. O teste não tem a pretensão de substituir a utilização dos métodos tradicionais, como culturas e pesquisas diretas, mas sim corroborar como diagnóstico complementar.
Referências bibliográficas
1. WHO fact sheets, the top 10t causes of death. May 2018.https://www.who.int/news-room/fact-sheets/detail/the-top-10-causes-of-death.
2. Lee AH et al, Performance of a multiplex PCR pneumonia panel for the identification of pathogens and the main determinants of resistancefrom the lower respiratory tract specimens of adult patients in intensive care units, J Microgiol Immunol Infect, 2019, 52.
3. Jain S et al, Community-acquired pneumonia requiring hospitalization among U.S. adults, N Engl J Med, 2015, 373.
4. Buchan BW et al, Practical composition of the BioFire®FilmArray®Pneumonia Panel to routine diagnostic methods and potential impact on antimicrobial stewardship in adult hospitalized patients with lower respiratory tract infections, J Clin Microbiol. Doi:10.11128/JCM.00135-20, April 2020.
5. Kalil AC et al, Management of Adults with Hospital-acquired and Ventilator-associated Pneumonia: 2016 Clinical Practice Guidelines by the Infectious Disease Society of America and the American Thoracic Society. Clin Infect Dis, 63(5)
6. Chastre J, Fagon JY: 2002. Ventilator-associated pneumonia. Am J Respir Crit Care Med, 876 165(7):867-903. 877
7. Tamma PD, Goodman KE, Harris AD, Tekle T, Roberts A, Taiwo A, Simner PJ: 2017. Comparing 878 the Outcomes of Patients With Carbapenemase-Producing and Non-Carbapenemase-Producing 879 Carbapenem-Resistant Enterobacteriaceae Bacteremia. Clin Infect Dis, 64(3):257-264.
8. Murphy C N et al, Multicenter Evaluation of the BioFire FilmArray Pneumonia/Pneumonia Plus Panel for Detection and Quantificationof Agents of Lower Respiratory Tract Infection, J Clin Microbiol, 2020 Jul 54(7).
9. Buchan B W, Practical Comparison of the BioFire FilmArray Pneumonia Panel to Routine Diagnostic Methods and Potential Impact on Antimicrobial Stewardship in Adult Hospitalized Patients with Lower Respiratory Tract Infections, J Clin Microbiol, 2020 Jul 58(7).
